fizyka.pisz.pl
forum zadankowe
matematyka w fizyce
kinematyka
dynamika
ruch obrotowy
pole grawitacyjne
teoria względności
siły sprężystości i drgania mechaniczne
fale mechaniczne
akustyka
elektrostatyka
prąd elektryczny
magnetyzm
indukcja i fale elektromagnetyczne
optyka
światło i atom
termodynamika
hydrostatyka
ciało stałe
przemiany jądrowe
gra w kropki
termodynamika - przemiana ciepła / pracy
fizykadasielubic:
 Witam, przychodzę o pomoc w takim oto zadaniu.
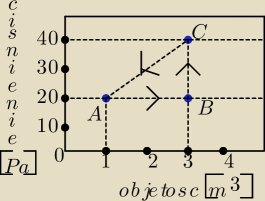
Układ termodynamiczny poddano przemianom od stanu początkowego A do B,
od B do C i od C do A.
Mam do uzupełnienia ( + , − , 0) taką oto tabelkę :
−−−−−−−−−−−−−−−−−−−−−−−−−
| | Q | W | ΔEw |
| A −> B | | | + |
| B −> C | + | | |
| C −> A | | | |
−−−−−−−−−−−−−−−−−−−−−−−−−
Oraz obliczyć wartość całkowitej pracy wykonanej przez układ w tym zamkniętym cyklu.
Witam, przychodzę o pomoc w takim oto zadaniu.
Układ termodynamiczny poddano przemianom od stanu początkowego A do B,
od B do C i od C do A.
Mam do uzupełnienia ( + , − , 0) taką oto tabelkę :
−−−−−−−−−−−−−−−−−−−−−−−−−
| | Q | W | ΔEw |
| A −> B | | | + |
| B −> C | + | | |
| C −> A | | | |
−−−−−−−−−−−−−−−−−−−−−−−−−
Oraz obliczyć wartość całkowitej pracy wykonanej przez układ w tym zamkniętym cyklu.
czyli minusik.
Pracę liczymy ze wzoru W = p(V2 − V1) = 20 *(3−1) = 20*2 = 40 J, czyli do pracy też leci
plusik.
W B −−> C mamy izochorę, a w takiej przemianie z definicji nie wykonuje się żadna praca.
Z I zasady termodynamiki mamy U = Q + W, ale w izochorze W = 0.
W takim razie ponieważ w treści było podane, że w tej przemianie ciepło jest dodatnie, to z
przekształconego wzoru U = Q + 0,
wychodzi że energia również będzie tutaj dodatnia, a więc plusik.
Tą część udało mi się zrobić, ale zupełnie nie wiem jak zabrać się za przemianę C −−> A, także
proszę o pomoc.
 Witam, przychodzę o pomoc w takim oto zadaniu.
Układ termodynamiczny poddano przemianom od stanu początkowego A do B,
od B do C i od C do A.
Mam do uzupełnienia ( + , − , 0) taką oto tabelkę :
−−−−−−−−−−−−−−−−−−−−−−−−−
| | Q | W | ΔEw |
| A −> B | | | + |
| B −> C | + | | |
| C −> A | | | |
−−−−−−−−−−−−−−−−−−−−−−−−−
Oraz obliczyć wartość całkowitej pracy wykonanej przez układ w tym zamkniętym cyklu.
Witam, przychodzę o pomoc w takim oto zadaniu.
Układ termodynamiczny poddano przemianom od stanu początkowego A do B,
od B do C i od C do A.
Mam do uzupełnienia ( + , − , 0) taką oto tabelkę :
−−−−−−−−−−−−−−−−−−−−−−−−−
| | Q | W | ΔEw |
| A −> B | | | + |
| B −> C | + | | |
| C −> A | | | |
−−−−−−−−−−−−−−−−−−−−−−−−−
Oraz obliczyć wartość całkowitej pracy wykonanej przez układ w tym zamkniętym cyklu.
| V | ||
W A −−> B mamy izobarę. Ponieważ | = const a objętość nam rośnie, to ciepło musi spadać | |
| T |
14 maj 19:51
'Leszek: Przede wszystkimzalezy to od " umowy" w niektorych podrecznikach podane jest , ze
jezeli ogrzewamy gaz to Q> 0 , jezeli nad gazem wykonujemy prace to W> 0 , jezeli
rosnie temperatura to ΔEw > 0
Przy takiej umowie otrzymujemy :
A→B : p = const. V rosnie , T rosnie , ogrzewamy gaz Q>O , W< 0 bo gaz wykonuje prace
przeciwko sila zewnetrznym , ΔEw > 0
B →C : V = const. p rosnie , T rosnie ogrzewanie gazu , Q>0 , W= 0 , ΔEk >0
C→A: p maleje ,V maleje , T maleje oziembianie gazu , Q< 0 , W< 0 , ΔEk <0
Calkowita praca rowna jest polu trojkata : W= 0,5*( 40 − 20)(3 − 1) = 20 J
14 maj 20:47
fizykadasielubic:
Dziękuję za szybką odpowiedź!
Jeżeli można, to czy mógłbym prosić jeszcze o dokładniejsze wytłumaczenie sytuacji C −−> A?
Chodzi mi o zrozumienie schematu, żebym mógł dalej sam rozwiązywać podobne zadania w
domu/szkole.
Pierwsze dwie przemiany są logiczne (chociaż nie zauważyłem swojego błędu z pracą w pierwszej
przemianie, dziękuję za poprawienie mnie), ale trzecia jest dość myląca.
Nie jest to izoterma/izobara/izochora, więc nie wiem jakiego wzoru tu użyć, a na wyczucie
jeszcze tego nie łapię.
14 maj 22:06
'Leszek: Wszystkie zmiany sprawdzamy z rownania stanu gazu np.
C→A to nie jest zadna ze znanych przemian wiec nie szukaj jej nazwy , ale zauwaz ,ze
pA < pC oraz VA < VC czyli TA < TC , cieplo jest odbierane .
| pA*VA | pC*VC | ||
= | |||
| TA | TC |
14 maj 22:29
fizykadasielubic:
Rzeczywiście, a skoro ciepło jest odbierane, to układ musi wykonywać jakąś pracę żeby tracić to
ciepło, a więc praca będzie ujemna.
Skoro i praca i ciepło są ujemne, to z I zasady termodynamiki również energia musi być ujemna.
O to chodziło? Dobrze myślę?
Czy da się do takich rozwiązań dojść bardziej ,,oficjalnie" ( z jakiegoś dowodu/wzoru), czy
(nie)stety trzeba tutaj po prostu myśleć logicznie i w ten sposób dojść do rozwiązania?
Dziękuję za pomoc!
14 maj 23:16
||: Myślec trzeba zawsze i..do końca w C→A Q < 0 ale W > 0 czyli znak Ew zalezy od tego który z tych składników jest większy,
sprawdź to !
w C→A Q < 0 ale W > 0 czyli znak Ew zalezy od tego który z tych składników jest większy,
sprawdź to !
 w C→A Q < 0 ale W > 0 czyli znak Ew zalezy od tego który z tych składników jest większy,
sprawdź to !
w C→A Q < 0 ale W > 0 czyli znak Ew zalezy od tego który z tych składników jest większy,
sprawdź to !
15 maj 10:40
'Leszek: Energia wewnetrzna Ew jest wprostproporcjonalna do zmany temperatury
ΔEw = ncv *ΔT , jak rosnie temperatura to ΔEw > 0
W przemianie C→A temperatura maleje ( wynika to z rownania stanu gazu )wiec ΔEw < 0
15 maj 11:04
fizykadasielubic: Teraz juz wszystko jasne, bardzo dziękuję za pomoc
15 maj 11:15
123: @110:04 to I zas. termodynamiki w tym przypadku nie obowiązuje ?
15 maj 14:35
'Leszek: I zasada termodynamiki obowiazuje , to jedna z najbardziej podstawowych zasad fizyki ,
gdzie Ty widzisz , ze w przemianie C→ A ta zasada nie obowiazuje ?
15 maj 17:27
daras: @fizykadasielubic wyciągasz błędne wnioski:
19:51 cytuję:
"W A −−> B mamy izobarę. Ponieważ p = const a objętość nam rośnie, to ciepło musi spadać czyli
minusik."
Nie minusik lecz plusik, bo temperatura (w kelwinach) rośnie proporcjonalnie do objętości.
i dalej:
"W takim razie ponieważ w treści było podane, że w tej przemianie ciepło jest dodatnie, to z
przekształconego wzoru U = Q + 0, wychodzi że energia również będzie tutaj dodatnia, a więc
plusik."
Tutaj dobrze ale nie wynika to z tego, że zaznaczono w tabelce plusik lecz z tego, że
wzrosła temperatura gazu Tc > TB > Ta
@'Leszek
20:47
"C→A: p maleje ,V maleje , T maleje oziembianie gazu , Q< 0 , W< 0 , ΔEk <0"
Jeśli traktujemy pracę sił zewnętrznych jako dodatnią to w tej przemianie W > 0.
Czyli słusznie jak zaznaczył || znak ΔU będzie zależał od porównania tej pracy z ilością
oddanego ciepła.
15 maj 18:29
anon: Czy pracy w przemianie C −−> A nie możemy policzyć z całki ∫CA pdV? Wtedy wynik wychodzi
ujemny.
15 maj 19:45
'Leszek: Dla gazu doskonalego energia wewnetrzna jest : U = ncv * T , jezeli maleje T , maleje U
czyli ΔU < 0 , natomiast problemy moga byc z praca W , w niektorych podrecznikach
spotykam , ze jezeli gaz wykonuje prace przeciwko sila zewnetrznym to W < 0
lub w innym podreczniku , ze jest odwrotnie , ale z energia wewnetrzna nigdy tak nie ma .
15 maj 21:33
jg: Małe pytanie nie w temacie, ktoś robi pracę domową nr 4 na pewnej politechnice? 

15 maj 22:04
fizykadasielubic: Nie zaprzeczam, nie zaprzeczam 

15 maj 22:36