fizyka.pisz.pl
forum zadankowe
matematyka w fizyce
kinematyka
dynamika
ruch obrotowy
pole grawitacyjne
teoria względności
siły sprężystości i drgania mechaniczne
fale mechaniczne
akustyka
elektrostatyka
prąd elektryczny
magnetyzm
indukcja i fale elektromagnetyczne
optyka
światło i atom
termodynamika
hydrostatyka
ciało stałe
przemiany jądrowe
gra w kropki
przemiana gazu doskonałego
Noname: Jaką pracę wykona 8 moli jednoatomowego gazu doskonałego w przemianie izobarycznej, jeżeli
temperatura wzrosła o 25 K ?
13 cze 17:19
Leszek: praca w przemianie izobarycznej gazu doskonałego
W=p*ΔV=p(V1−V2)
zatem po podstawieniu do W =nR(T1−T2) = nRΔT
W=1662 J
| nRT1 | ||
na podstawie równania Clapayrona : pV1=nRT1 => V1= | ||
| p |
| nRT2 | ||
pV2=nRT2 => V2= | ||
| p |
13 cze 20:49
Leszek:
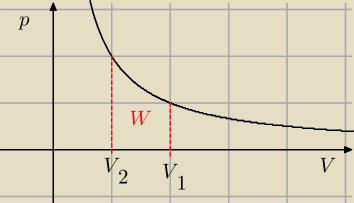 ZADANIE
obliczyć pracę wykonaną podczas sprężania izotermicznego gazu od objętości
ZADANIE
obliczyć pracę wykonaną podczas sprężania izotermicznego gazu od objętości
t=27o C , temperatura gazu
V1
V2
W= 249,3*ln2 [J]
 ZADANIE
obliczyć pracę wykonaną podczas sprężania izotermicznego gazu od objętości
ZADANIE
obliczyć pracę wykonaną podczas sprężania izotermicznego gazu od objętości
| J | ||
V1= 2 dm3 do V2=1 dm3 ; ilość moli gazu n =0,1 ; stała gazowa R=8,31 [ | ] | |
| mol*K |
| nRT | nRT | |||
dW=pdV ale p= | czyli dW= | *dV | ||
| V | V |
| dV | V1 | |||
zatem W = nRT ∫ | = nRTln( | ) | ||
| V | V2 |
15 cze 21:41
http://www.matematyka.pl/40879: http://www.matematyka.pl/408794.htm#p5436581
16 cze 08:25